Данные Реальной Клинической Практики (Real World Data) в онкологии: ЧАСТЬ 1
Автор: Овчинников Дмитрий Александрович, кандидат биологических наук, эксперт в фармразработке
Создание новых лекарственных средств (ЛС) в эру доказательной медицины покоится на 4 столпах: фармацевтическая разработка, доклинические исследования, контролируемые рандомизированные клинические исследования (РКИ) и регистрация в уполномоченном органе, включающая анализ и оценку всех полученных данных и процесса производства. Первые шаги к пониманию важности всех этих элементов были сделаны в прошлом веке, но эта дорога не была простой. На этом пути хватало трагических поворотов (сульфаниламидная1 или талидомидовая2 трагедии) и преступлений (незаконные эксперименты нацистских врачей3), но общими усилиями врачей, ученых, пациентов и общественных деятелей удалось создать разумную систему контроля за созданием новых ЛС и оценки их риска/пользы, а затем описать ее в документах Международной конференции по Гармонизации (ICH), так называемых GxP руководствах и их национальных аналогах.
Однако со временем стали видны проблемы и недостатки классических клинических исследований (КИ). Выделим 3 наиболее важных, хотя сложностей больше.
- Очень длительный период разработки, требующий огромных инвестиций. По последним оценкам университета Дюка4, стоимость вывода одного препарата на рынок уже превысила 2 млрд долларов США. Возврат таких инвестиций – сложная задача даже для транснациональных корпораций, а стоимость инновационных ЛС ложится тяжким бременем на плечи государства и пациентов, ограничивая их доступ к новым методам терапии.
- Требование о статистической достоверности КИ при всей своей разумности и обоснованности существенно осложняет или даже делает невозможной разработку ЛС для орфанных заболеваний или небольших пациентских субпопуляций — например, для пациентов, несущих специфическую мутацию в гене, кодирующем какой-то белок. Набор и наблюдение нескольких тысяч пациентов, необходимые для всесторонней оценки препарата, могут быть невозможны (или потребуют слишком длительных, а значит и дорогих исследований), если в мире в общей сложности насчитывается всего несколько тысяч таких больных.
- В ходе КИ собираются данные от «идеализированных пациентов», существенно отличающихся от пациентов, с которыми сталкивается врач в своей ежедневной практике. С одной стороны, это помогает четче оценить профиль безопасности/эффективности разрабатываемого ЛС, с другой – приводит к существенному расхождению между результатами КИ и реальной клинической практикой.
Хотя идеального решения этих вопросов пока не найдено, развитие науки и технологий указали один из возможных путей – это анализ Данных Реальной Клинической Практики (ДРКП) или Real World Data.
Давайте сначала разберемся, что такое ДРКП, откуда они берутся, какие проблемы призваны решить, коснемся проблем и ограничений ДРКП, а затем во второй части посмотрим на первые успехи этого подхода, который уже показал свой потенциал во многих странах мира.
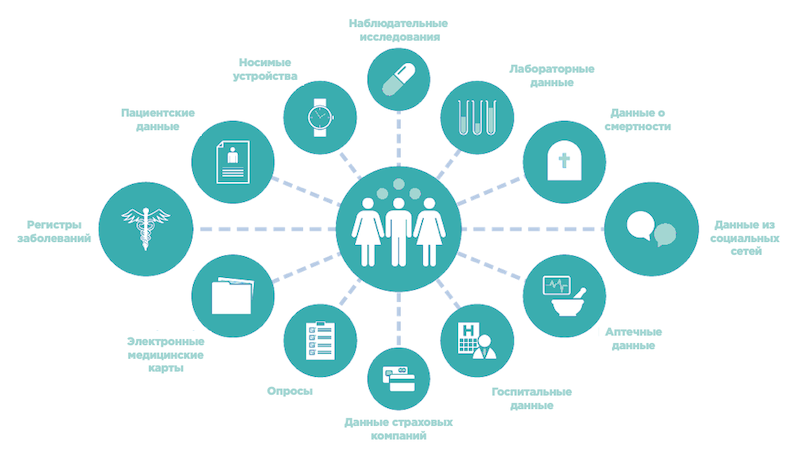
Источники ДРКП
ДРКП можно определить как данные, полученные в рутинной клинической практике при применении ЛС у пациентов. Источниками ДРКП являются:
- Электронные медицинские карты и записи;
- Базы данных страховых компаний и выставления счетов за медицинские услуги (billing activities);
- Данные из системы фармаконадзора;
- Аптечные данные по учету рецептурных заказов;
- Разнообразные пациентские, продуктовые регистры и регистры заболеваний;
- Социальные сети, включая блоги и сайты пациентских сообществ;
- Данные, генерируемые пациентом самостоятельно, включая:
• Данные с носимых устройств, фиксирующих состояние пациента (фитнес-трекеры, инсулиновые датчики, мобильные телефоны и т. д.);
• Дневники пациентов и аналогичные записи самооценки состояния;
• Результаты лечения по оценке пациента (Patient-oriented Outcome).
Особое значение в последнее время приобретают данные, полученные из социальных сетей, и так называемые Результаты лечения по оценке пациента. Это совершенно новый подход к изучению эффектов ЛС, основанный на самостоятельной оценке пациентами результатов лечения. Это логичное продолжение концепции по оценке качества жизни – Quality of Life (QoL), получившей очень ограниченное использование в российской практике, но пользующейся большим спросом на Западе.
Американский регулятор FDA, опубликовавший наибольшее количество регуляторных документов по использованию ДРКП, рекомендует не включать данные из КИ в понятие ДРКП5, хотя оставляет возможность их использования при анализе данных из наблюдательных программ и эпидемиологических исследований с минимальным влиянием на выбор врача/пациента.
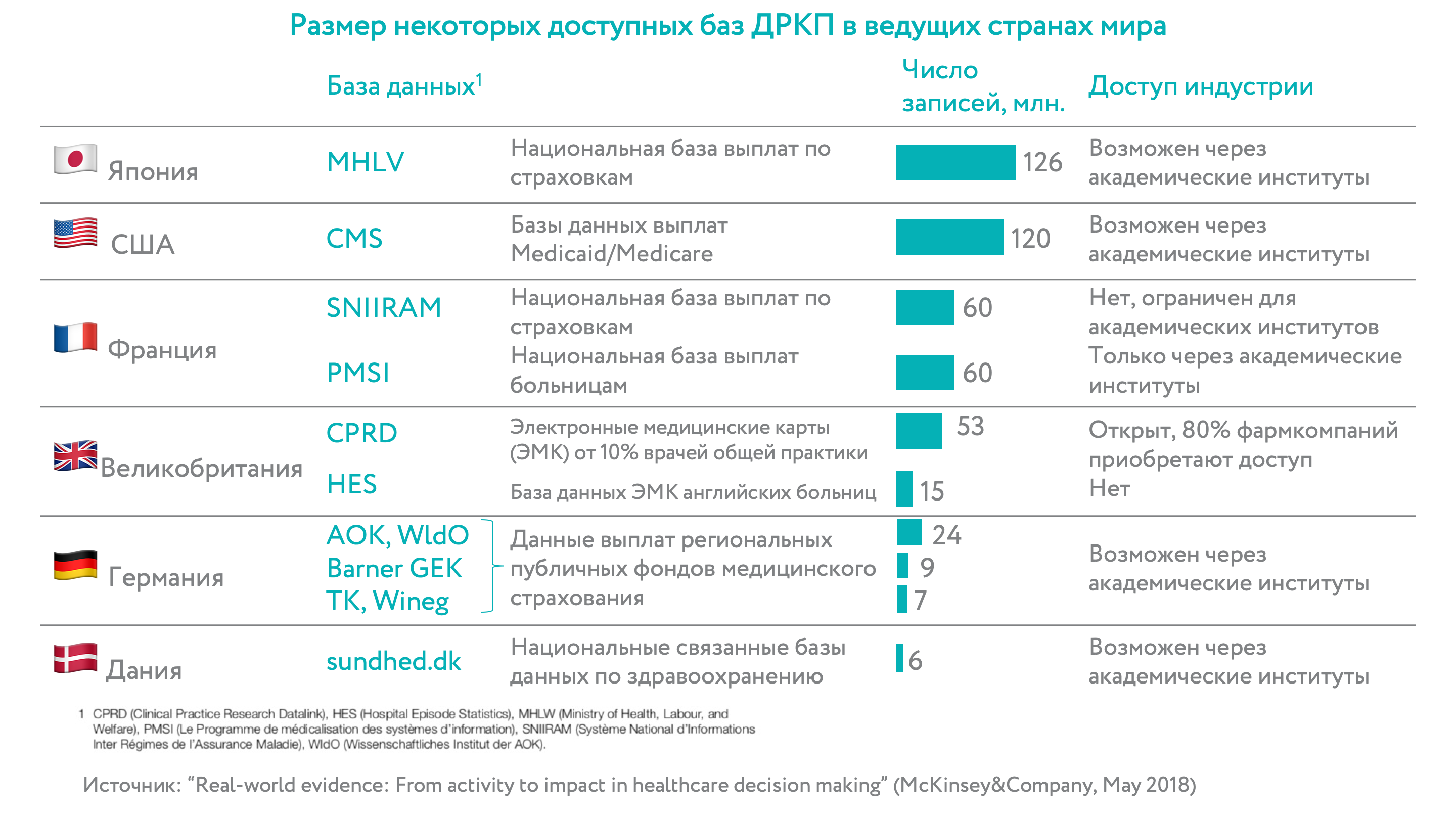
С появлением компьютерных систем ведения медицинских записей объём ДРКП стал лавинообразно нарастать, и сейчас ведущие базы данных уже обладают сотнями миллионов уникальных пациентских записей. Появившиеся новые статистические методы анализа, технологии Data Sciences (наука о данных) и нейросетевое программирование привели к созданию инструментов для обработки и анализа таких массивов данных, чтобы выявить закономерности, тренды и важные факторы, предсказывающие успех/неуспех лечения.
Почему ДРКП так популярны?
Помимо моды на все новое, которая иногда захлестывает и ученых, ДРКП обладают несколькими свойствами, делающими их потенциально важным инструментом в разработке и оценке ЛС.
- Сбор ДРКП происходит параллельно реальной практике, и почти не требует дополнительных расходов на генерацию данных.
Для появления большинства ДРКП — в отличие от КИ — не нужно писать протоколы (в случае наблюдательных исследований предварительное одобрение Протокола все же необходимо), одобрять их в регуляторном органе и давать пациентам препараты бесплатно. Повседневная медицинская деятельность сама будет генерировать ДРКП при условии установки систем электронных медицинских записей и интеграции лабораторного комплекса. Процессы цифровизации медицины идут самостоятельно и не ложатся тяжким грузом на бюджет исследования.
Сбор данных с носимых устройств или из аптечных систем также не требуют расходов. Владельцы данных могут продавать их для анализа, но расходы на приобретение такой базы все равно будут не сопоставимы с расходами на включение 1 пациента в РКИ.
- Высокая скорость получения результата.
Так как ДРКП генерируются самопроизвольно и содержат истории пациентов с самыми разнообразными заболеваниями и состояниями, то для ответа на любой научный вопрос достаточно лишь получить доступ к базе данных, иметь алгоритм обработки данных и хорошие вычислительные мощности. Таким образом, ответ может быть получен в течение считанных дней (при условии наличия базы данных).
Особое значение это приобретает для оценки каких-либо отдаленных эффектов (профилактика возникновения заболевания или рецидива, истинная выживаемость вместо пятилетней). В ходе РКИ изучение таких эффектов – очень долгое и дорогое удовольствие, и это вынуждает изучать суррогатные конечные точки. Лучшие из баз ДРКП на сегодняшний день уже охватывают более 10 лет наблюдения, это позволяет оперативно оценивать длительные эффекты терапии. При этом сбор информации продолжается, и скоро глубина баз данных достигнет продолжительности человеческой жизни.
- Множество исследований – одна база.
В базе данных ДРКП будет регистрироваться медицинская информация от любых пациентов с самыми разными заболеваниями, поэтому одну и ту же базу (при условии значительного размера) можно использовать для изучения разных препаратов или болезней снова и снова.
- Широкий охват исходов лечения.
Универсальность данных помогает решать и другую проблему РКИ – узкий спектр оценки. При написании протокола автору приходится формулировать гипотезу об эффекте препарата, и в зависимости от нее фиксировать небольшое количество конечных точек исследования (например, выживаемость или снижение какого-то биологического маркера), по которым будет оцениваться эффективность ЛС. Но препарат может влиять на выбранные конечные точки незначительно, в то же время существенно улучшая какие-то другие терапевтически важные и значимые параметры (другие маркеры, время до прогрессии и т. д.). Анализируя ДРКП, можно оценить изменения практически любого количества конечных точек и увидеть действия ЛС во всей полноте.
- Реальные пациенты – реальный эффект.
Наиболее содержательным и трудно разрешимым возражением против РКИ является тот факт, что в них включают только «идеализированных пациентов», прошедших сквозь сито критериев включения и исключения. Это позволяет лучше проследить эффекты применения препарата на относительно небольшой популяции, но в реальной практике как эффективность, так и безопасность ЛС могут сильно отличаться. Пациенты в реальной практике болеют многими заболеваниями, принимают множество препаратов и БАДов, а уровень их приверженности лечению и частота наблюдений сильно варьируют. Все это приводит к разнице между эффективностью и безопасностью препаратов, показанными в ходе РКИ и в реальной практике. Особенно важно, что ДРКП позволяют получить данные от особых пациентских групп (детей, беременных женщин и т. д.), включение которых в РКИ затруднено.
- ДРКП незаменимы при экономической оценке дорогостоящих схем лечения.
Разница между реальной практикой и результатами РКИ стала приобретать особое значение с выходом на рынок сверхдорогих ЛС стоимостью в сотни тысяч долларов США для лечения рака или орфанных заболеваний. Если заявленная эффективность сильно выше реальной, то фармакоэкономические модели, положенные в основу согласованной цены, неверны, и система здравоохранения существенно переплачивает. Экономика здравоохранения — один из основных «заказчиков» исследований ДРКП в настоящее время.
Проблемы и ограничения.
Безусловно, анализ ДРКП имеет свои ограничения, но многие из них могут быть устранены общими усилиями ученых, регуляторов и медицинского сообщества.
Хотя отдельные примеры использования ДРКП прослеживаются с середины прошлого века, систематический сбор баз данных начался недавно. Глубина наблюдения приближается в настоящее время к 10 годам, а количество записей для лучших баз данных уже превышает 100 млн. С учетом неполноты записей, разных стандартов ведения и лечения пациентов, сбор достаточной для анализа единообразной выборки остается непростой задачей. Эта проблема, безусловно, будет преодолена со временем, сейчас и FDA, и EMA рекомендуют объединять несколько разных баз данных для формирования гомогенной выборки нужного размера.
Права доступа даже к анонимизированной медицинской информации сильно отличаются в разных странах мира, это препятствует объединению баз и проведению международных исследований. Многие из баз данных были сформированы без надлежащего согласия/уведомления пациентов или способом, который не признан на территории других стран, что требует от заказчика исследования особой аккуратности при выборе источников данных. Трансграничная передача такой информации контролируется специальными и очень запутанными законами как в США и Европе, так и в РФ. Здесь необходимо запустить процесс по гармонизации условий получения согласия на сбор, хранение и передачу информации из баз ДРКП аналогичный тому, который был сделан для КИ в рамках ICH.
Аналогично, отсутствует консенсус о приемлемых и правильных алгоритмах/подходах к нормированию баз данных, их анализу и методам представления результатов. Хотя работа по формализации этой области уже начата как регуляторами, так и научным сообществом, требуется ускорить работу в этом направлении. Классические статистические подходы, используемые для анализа РКИ, малоприменимы для анализа ДРКП и должны быть существенно переработаны с учетом гетерогенности данных, их неполноты, потенциального задвоения данных и разнообразия оцениваемых переменных.
Низкий уровень доверия к результатам анализа ДРКП среди экспертов и регуляторов сдерживает развитие этого подхода, который может органично дополнить имеющиеся инструменты по оценке профиля эффективности и безопасности ЛС. С этой проблемой помогут справится новые исследования по сопоставимости данных РКИ и ДРКП, включение анализа ДРКП в регуляторные документы по примеру рамочной программы FDA6 и популяризация подхода в экспертном сообществе (через обучение и распространение информации об успехах и ограничениях нового метода).
Список использованной литературы:
- Paine MF., Clin Pharmacol Ther. 2017 Apr;101(4):430-434 https://ascpt.onlinelibrary.wiley.com/doi/abs/10.1002/cpt.613
- Kim JH, Scialli AR., Toxicol Sci. 2011 Jul;122(1):1-6 https://academic.oup.com/toxsci/article/122/1/1/1672454
- Paul Weindling et al., Endeavour. 2016 Mar; 40(1): 1–6. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4822534/
- Joseph A. DiMasi et al., Journal of Health Economics, (47) 2016 https://www.sciencedirect.com/science/article/abs/pii/S0167629616000291?via%3Dihub
- Use of Real-World Evidence to Support Regulatory Decision-Making for Medical Devices, Guidance for Industry and FDA Staff, August 2017 https://www.fda.gov/regulatory-information/search-fda-guidance-documents/use-real-world-evidence-support-regulatory-decision-making-medical-devices
- Framework for FDA’s Real-World Evidence Program, Декабрь 2018 https://www.fda.gov/media/120060/download
- Медвестник. Расходы на здравоохранение в мире достигнут к 2022 году 10 трлн долл. – прогноз. 11 февраля 2019 https://medvestnik.ru/content/news/Rashody-na-zdravoohranenie-v-mire-dostignut-k-2022-godu-10-trln-doll-prognoz.html
- Фармацевтический вестник. Эксперт: необходимо внедрить систему оценки технологий здравоохранения. 29 июня 2019 https://pharmvestnik.ru/content/news/Ekspert-neobhodimo-vnedrit-sistemu-ocenki-tehnologii-zdravoohraneniya.html
- Prostate Cancer UK. Earlier abiraterone finally approved for men in England and Wales. 21 Mar 2016 https://prostatecanceruk.org/about-us/news-and-views/2016/3/earlier-abiraterone-finally-approved-for-men-in-england-and-wales
- Business Wire. Janssen Presents Newly-Published Data on the Use of ZYTIGA® (Abiraterone Acetate) Plus Prednisone in the Real-World, Outside the Clinical Trial Setting. February 17, 2017 https://www.europeanmedical-group.com/omnipresent/janssen-presents-newly-published-data-on-the-use-of-zytiga-abiraterone-acetate-plus-prednisone-in-the-real-world-outside-the-clinical-trial-setting/
- Ramaekers BLT et al., Pharmacoeconomics. 2017 Feb;35(2):191-202 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5253156/
- Medical News Today. NICE recommends abiraterone for prostate cancer. 21 March 2016 https://www.medicalnewstoday.com/releases/308158.php
- William C.N. Dunlop et al., Health Policy. 2018 May; 122 (5): 528-532 https://www.sciencedirect.com/science/article/pii/S0168851018300514#bib0055
- Celgene a conclu un accord «efficace ou remboursé» avec le CEPS pour Imnovid. February 15, 2015 https://www.apmnews.com/Celgene-a-conclu-un-accord-efficace-ou-rembourse-avec-le-CEPS-pour-Imnovid-FS_256638.html
- NICE Technology appraisal guidance TA129. Bortezomib monotherapy for relapsed multiple myeloma. 23 October 2007 https://www.nice.org.uk/guidance/TA129/chapter/3-The-manufacturers-submission
- Е. Крючкова, Коммерсант. №60 от 07.04.2017: 2 https://www.kommersant.ru/doc/3263496
- Kristin M. Sheffield et al., Am J Health Syst Pharm. 2017 Jun 1;74(11):832-842 https://academic.oup.com/ajhp/article/74/11/832/5102793
- Tackling RWE Challenges To Demonstrate Healthcare Value. 2 января 2018 https://scrip.pharmaintelligence.informa.com/SC100133/Tackling-RWE-Challenges-To-Demonstrate-Healthcare-Value
- The Sentinel Initiative. https://www.sentinelinitiative.org/background
- Пресс-релиз компании Pfizer от 3 февраля 2015 https://www.pfizer.com/news/press-release/press-release-detail/pfizer_receives_u_s_fda_accelerated_approval_of_ibrance_palbociclib
- Фармацевтический вестник. FDA одобряет применение Ibrance у пациентов мужского пола с раком молочной железы. 5 апреля 2019 https://pharmvestnik.ru/content/news/FDA-odobryaet-primenenie-Ibrance-u-pacientov-mujskogo-pola-s-rakom-molochnoi-jelezy.html
- Пресс-релиз компании Pfizer от 4 апреля 2019 https://www.pfizer.com/news/press-release/press-release-detail/u_s_fda_approves_ibrance_palbociclib_for_the_treatment_of_men_with_hr_her2_metastatic_breast_cancer
- The Cancer Letter., How real world evidence was used to support approval of Ibrance for male breast cancer. Apr. 19, 2019 https://cancerletter.com/articles/20190419_2/
- Nancy A. Dreyer., Ther Innov Regul Sci. 2018 May; 52(3): 362–368. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5944086/#bibr16-2168479018763591
- Cowey CL et al., Future Oncol. 2017;13:1699–1710. https://www.futuremedicine.com/doi/10.2217/fon-2017-0187?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%3dwww.ncbi.nlm.nih.gov
- Becker JC et al., Oncotarget. 2017;8:79731–79741. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5668086/
- Пресс-релиз European Medicines Agency. New cell-based therapy to support stem cell transplantation in patients with high-risk blood cancer. 2016, June 24. http://www.ema.europa.eu/ema/index.jsp?curl=pages/news_and_events/news/2016/06/news_detail_002555.jsp&mid=WC0b01ac058004d5c1.
- Gökbuget N. et al., Blood Cancer J. 2016 Sep 23;6(9) https://www.nature.com/articles/bcj201684
- Пресс-релиз Friends of Cancer Research «Establishing a Framework to Evaluate Real-World Endpoints» от 10 июля 2018 https://www.focr.org/sites/default/files/RWE_FINAL%207.6.18.pdf?eType=EmailBlastContent&eId=45c28471-3adc-4f10-baa5-2b1181858d97